Анемия при язвенном колите: факторы риска и оптимизация терапии
Оригинальная статья/Original Article УДК 616.348-002
Тема: Анемия при язвенном колите: факторы риска и оптимизация терапии
Авторы: Т. Е. ЧЕРНЫШОВА 1, С. Н. СТЯЖКИНА 1, А. А.ВАЛИНУРОВ 2,
В. В. СОКОЛОВА 1
1 ФГБОУ ВО «Ижевская государственная медицинская академия» Минздрава России, Ижевск, Россия
2 Бюджетное учреждение здравоохранения Удмуртской Республики «Городская клиническая больница № 7 Министерства Здравоохранения Удмуртской Республики», Ижевск, Россия
Резюме
Введение. Дефицит железа или железодефицитная анемия (ЖДА) являются одними из наиболее распространённых системных осложнений воспалительных заболеваний кишечника (ВЗК). Такие симптомы, как усталость, снижение способности концентрироваться и снижение толерантности к физической нагрузке, могут имитировать общие симптомы ВЗК и поэтому могут легко игнорироваться. Многочисленные исследования показали, что анемия является основным фактором снижения качества жизни у пациентов с ВЗК. Однако коррекция анемии может значительно улучшить качество жизни пациентов с ВЗК. Поэтому рекомендуется, чтобы каждый пациент с ВЗК регулярно проходил скрининг на дефицит железа и анемию. При обнаружении следует начать соответствующее обследование и лечение. Цель исследования — проанализировать причины развития железодефицитной анемии (ЖДА) и анемии хронических заболеваний у пациентов язвенным колитом в Удмуртии. Материал и методы. Проведён анализ клинических протоколов, лабораторных и инструментальных данных 101 пациента с язвенным колитом в возрасте от 18 до 82 лет, включённых в «Республиканский регистр больных хроническими воспалительными заболеваниями кишечника» Удмуртии. Заключение. Анемия является наиболее распространённым системным осложнением у пациентов с ВЗК, к которым относится язвенный колит, в связи с чем ведутся поиски новых улучшенных методов диагностики и лечения анемии при язвенном колите.
Ключевые слова: язвенный колит; воспалительное заболевание кишечника; дефицит железа, железодефицитная анемия; коррекция анемии
Для цитирования: Чернышова Т. Е., Стяжкина С. Н., Валинуров А. А., Соколова В. В. Анемия при язвенном колите: факторы риска и оптимизация терапии. Антибиотики и химиотер. 2024; 69 (7-8): 37-43.
https://doi.org/10.37489/0235-2990-2024-69-7-8-37-43.
Anaemia in Patients with Ulcerative Colitis: Risk Factors and Therapy Optimization
TATYANA YE. CHERNYSHOVA1, SVETLANA N. STYAZHINA1, ARTUR A. VALINUROV2, VARVARA V. SOKOLOVA1
1 Izhevsk State Medical Academy of the Ministry of Health of the Russian Federation, Izhevsk, Russia
2 City Clinical Hospital No. 7 of the Ministry of Health of the Udmurt Republic, Izhevsk, Russia
Abstract
Background. Iron deficiency or iron-deficiency anaemia (IDA) are some of the most common systemic complications of inflammatory bowel diseases (IBD). Symptoms such as fatigue, reduced ability to concentrate, as well as decreased exercise tolerance can mimic common symptoms of IBD and therefore can be easily ignored. Numerous studies have shown that anaemia is a major contributor to reduced quality of life in patients with IBD. However, correction of anaemia can significantly improve the quality of life of patients with IBD. Therefore, it is recommended that every patient with IBD undergo regular screening for iron deficiency and anaemia. If they are detected, appropriate examination and treatment should be initiated. The aim of the study was to analyse the causes of IDA and anaemia for chronic conditions in ulcerative colitis patients in Udmurtia. Material and methods. Clinical protocols, laboratory and instrumental data of 101 patients with ulcer-ative colitis aged from 18 to 82 years included in the «Republican register of patients with chronic inflammatory bowel diseases» of Udmurtia were analysed. Results ofdiscussion. Anaemia is the most widespread systemic complication in patients with IBD, which includes ulcerative colitis. In this regard, new improved methods of diagnosing and treating anaemia in ulcerative colitis are being searched for.
Keywords: ulcerative colitis; inflammatory bowel disease; iron deficiency, iron-deficiency anaemia; anaemia correction
For citation: Chernyshova T. Ye., Styazhina S. N, ValinurovA. A, Sokoloval V. V. Anaemia in patients with ulcerative colitis: risk factors and therapy optimization. Antibiotiki i Khimioter = Antibiotics and Chemotherapy. 2024; 69 (7-8): 37-43.
https://doi.org/10.37489/0235-2990-2024-69-7-8-37-43.

Введение.
Воспалительные заболевания кишечника (ВЗК), объединяющие язвенный колит (ЯК) и болезнь Крона (БК), относятся к хроническим прогрессирующим аутоиммунным заболеваниям, поражающим преимущественно подвздошную и толстую кишку с развитием разнообразных кишечных и внекишечных проявлений [1-4]. Это одна из наиболее серьёзных и нерешённых проблем в современной гастроэнтерологии, что обусловлено высоким и постоянно растущим уровнем заболеваемости, недостаточно изученными факторами риска, непрогнозируемым течением и сложностями в выборе лечебной тактики.
Социальная значимость язвенного колита обусловлена преобладанием заболевания среди лиц молодого трудоспособного возраста, снижением качества жизни, высоким выходом пациентов на инвалидность [1, 4, 5].
К наиболее распространённым осложнениям ЯК относится анемия. Частота встречаемости анемии колеблется от 13 до 60% [6-8]. Известно, что анемия во многом определяет прогноз любого заболевания, в том числе язвенного колита, затрагивая качество жизни и трудоспособность пациентов, является частой причиной госпитализации, как в терапевтические, так и в хирургические отделения. Основной тип анемии у пациентов ЯК — железодефицитная анемия. Значительно реже регистрируется В12-дефицитная анемия [6-11].
В последние годы в литературе активно обсуждается проблема анемии хронических заболеваний (АХЗ), которая считается 2-й по частоте причиной развития анемии во всём мире [7, 12, 13].
В соответствии с пунктами 2.2.1. European Crohn's and Colitis Organisation Anaemia Consensus (2015) скрининг диагностики анемии включает: клинический анализ крови, определение уровня ферритина, процента насыщения трансферрина, подсчёт ретикулоцитов, сидероцитов, определение общего белка и белковых фракций, мочевины, креатинина, сывороточного железа, общей железосвязывающей способности сыворотки. В сложных случаях проводится исследование пунк-тата костного мозга и определение уровня витамина В12 и фолиевой кислоты в крови.
В табл. 1 приведены критерии дифференциальной диагностики основных вариантов анемии по показателям общего анализа крови, характерных для пациентов ЯК.
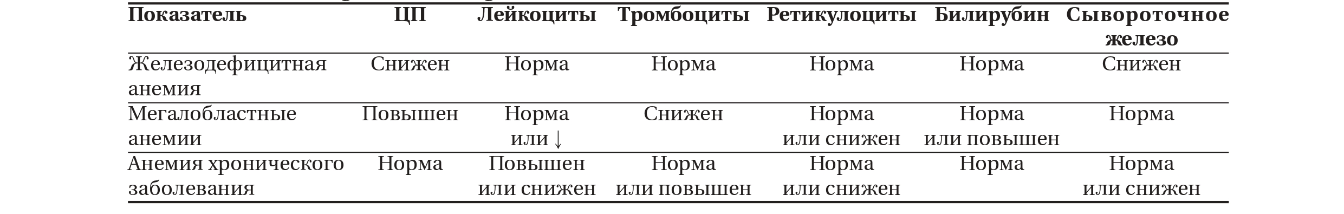 Таблица 1. Дифференциальная диагностика по показателям ОАК
Таблица 1. Дифференциальная диагностика по показателям ОАКЖелезодефицитная анемия (ЖДА) у пациентов ЯК выявляется с частотой от 18 до 52% [13]. Этиология ЖДА связана с потерями железа из язвенных дефектов желудочно-кишечного тракта, проблемами питания, возможным нарушением абсорбции железа и эритропоэза с формированием микроци-тарной гипохромной анемии [6, 10, 14].
Распространёнными симптомами ЖДА являются синдром беспокойных ног, глоссит, хейлоз и койлонихии, извращение вкуса с влечением к употреблению непищевых субстанций (например, льда, почвы, краски, крахмала, золы).
Лабораторные признаки ЖДА хорошо известны: микроцитоз, гипохромия, сниженный или нормальный уровень ретикулоцитов, снижение уровня сывороточного железа, ферритина и процента насыщения трансферрина с увеличением общей железосвязывающей способности сыворотки (ОЖСС).
При анализе причин ЖДА важно учесть особенности питания пациентов. Известно, что в продуктах животного происхождения железо двухвалентное, которое легко растворяется в щелочной среде тонкой кишки и хорошо всасывается. Железо из растительных продуктов трёхвалентное и для его поступления в кровоток необходимо, прежде всего, достаточное количество соляной кислоты в желудке, т. к. только в этом случае оно может стать двухвалентным и начать всасываться в тонком кишечнике.
У пациентов ЯК имеются особенности интерпретации значений уровня ферритина. При отсутствии клинических, эндоскопических или биохимических признаков активности болезни уровень ферритина ниже 30 мкг/л является достоверным признаком железодефицита, но при активности воспалительного процесса он может повышаться, несмотря на «пустые» запасы железа.
В12-дефицитная анемия — заболевание, связанное с дефицитом кобаламина, цианокобала-мина с характерным снижением количества эритроцитов и гемоглобина. У пациентов ЯК недостаток витамина В12 связан не только с патологией кишечника, но и сам вызывает его поражение, как и сопутствующие неврологические расстройства per se.
Витамин В 12 не синтезируется в организме, его запасы пополняются только за счёт пищи и, прежде всего, продуктов животного происхождения, таких как: мясо, субпродукты и морепродукты, а поступление в организм витамина В12 возможно только в присутствии внутреннего фактора Кастла, который синтезируется клетками слизистой оболочки желудка. Образовавшийся комплекс взаимодействует с рецепторами клеток слизистой оболочки подвздошной кишки, позволяя кобаламину попасть в кровь, связаться с транспортным белком — транскобаламином и поступить в костный мозг, где он участвует в процессе кроветворения.
Снижение кислотности желудочного сока — вторая важная причина нарушения всасывания витамина В12, как и длительный приём лекарственных средств, снижающих секрецию соляной кислоты, а также формирование синдрома мальабсорбции.
Третья причина — возможный аутоиммунный характер В12-дефицитной анемии, т. к. учитывая аутоиммунный генез ЯК, организм может продуцировать антитела не только против клеток желудка и кишечника, но и внутреннего фактора Кастла.
Для мегалобластной анемии характерен мак-рoцитoз. Однако при сочетании ЖДА с дефицитом витамина В12 размеры эритроцитов могут быть нормальными. Характерна гиперхромия. ОЖСС, отражающая количество железа, способного связаться с трансферрином, может быть нормальной или сниженнй, как и уровень рети-кулоцитов, но при этом уровень железа и фер-ритин в сыворотке крови регистрируется как нормальный или повышенный. Наиболее информативным методом доказательства дефицита витамина В12 является определение их концентрации в крови методом ИФА.
Анемия хронических заболеваний (АХЗ) — анемия, которая может быть обусловлена любой хронически протекающей инфекцией. Характерной чертой этого типа анемии является сочетание гипоферремии с достаточными его запасами в ре-тикулоэндотелиальной системе. В патогенезе АХЗ чаще всего сочетается несколько факторов, ведущих к снижению срока жизни эритроцитов с формированием блокады перехода железа из ре-тикулоэндотелиальных клеток в эритробласты и угнетением эритропоэза.
АХЗ характерна для заболеваний, связанных с активацией клеточного иммунитета, к которым относится ЯК. Новое в патогенезе АХЗ при ЯК — раскрытие роли провоспалительных цитокинов (IL1a, IL1b, TNFa) в экспрессии гепсидина печени. Гепсидин — железорегуляторный гормон печени, способствующий повышению естественной резистентности организма к инфекции, что
связано с его прямым бактерицидным действием и снижением доступности железа для микроорганизмов [13, 15-17] .
Цель исследования — оценить факторы риска развития анемии при язвенном колите и перспективы её коррекции препаратами гемового железа.
Материал и методы
Проанализированы амбулаторные карты и карты диспансерного наблюдения 101 пациента язвенным колитом в возрасте от 18 до 82 лет, включённых в «Республиканский регистр больных хроническими воспалительными заболеваниями кишечника» Удмуртской Республики.
Лабораторное исследование проведено на оборудовании Abbott (Германия). Ультразвуковое исследование органов брюшной полости и почек проводилось на аппарате «Esaote MyLab». Анализировался характер диеты, режим питания, тип нарушения пищевого поведения по опроснику «Оценка пищевого поведения» — DQEB (Dutch Questionnaire of Eating Behaviour). Всем пациентам проведена фиброгастродуоденоско-пия (ФГДС) с оценкой рН желудочного сока и морфологии слизистой, а также колоноскопия с забором не менее 4 био-птатов из отделов толстой и подвздошной кишки (как поражённых, так и интактных) с последующим гистологическим исследованием.
Статистическая обработка проведена с применением программы обработки электронных таблиц Microsoft Excel. Полученные в результате исследования данные обрабатывали общепринятыми методами вариационной статистики. Достоверность различий средних величин оценивали с помощью параметрических методов статистики (критерий Стьюдента). Разницу средних величин считали достоверной при р<0,05 (95% уровень значимости) и при р<0,01 (99% уровень значимости). С целью определения значимости различий применяли непараметрические критерий Вилкоксона (Т) для связанных совокупностей и критерий Вилкоксона-Мана-Уитни (U) для независимых совокупностей.
Результаты и обсуждение
При изучении историй болезни и амбулаторных карт пациентов ЯК на этапе формирования группы наблюдения выявлена высокая частота системной внекишечной патологии (табл. 2).
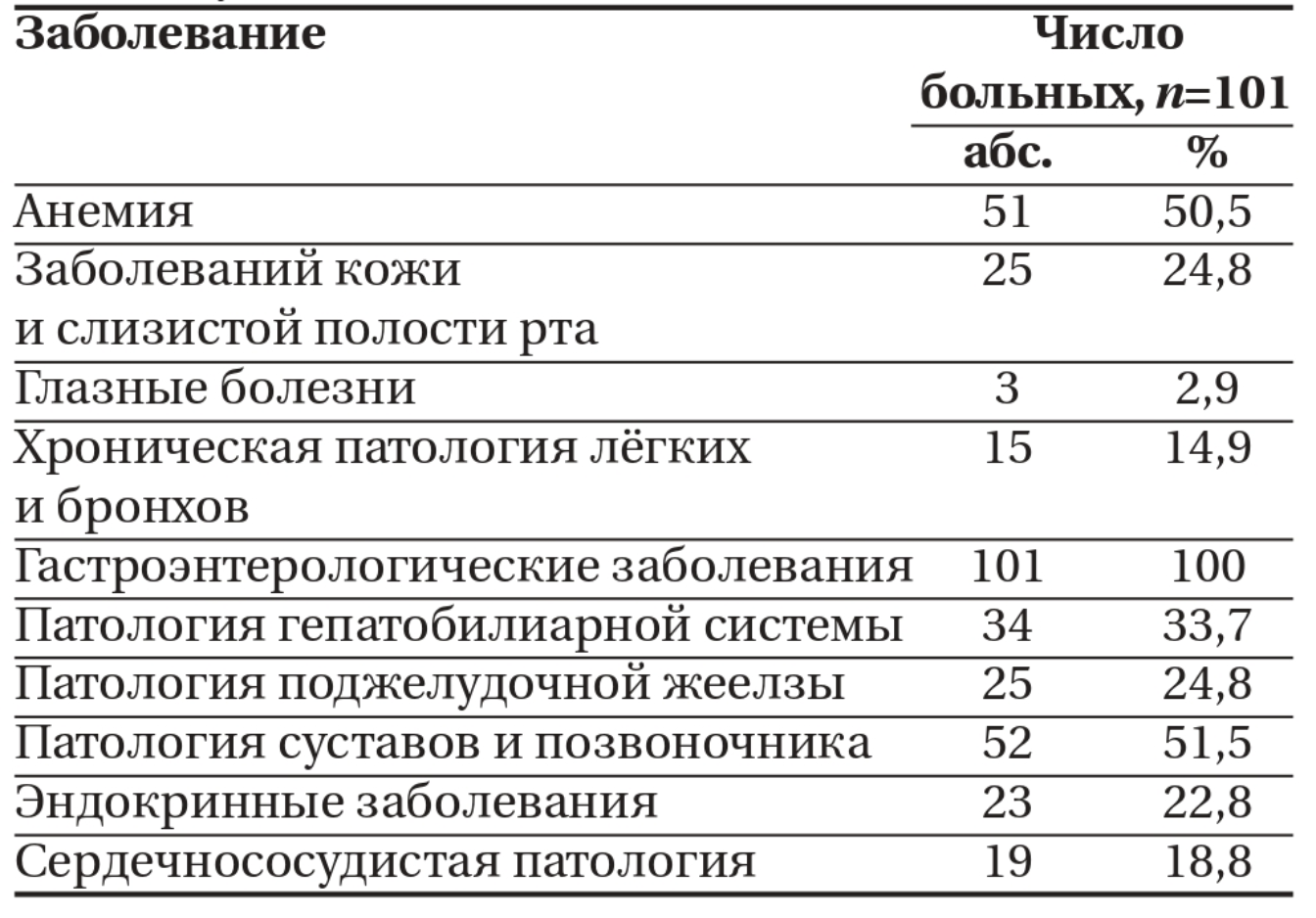 Таблица 2. Системные проявления язвенного колита
Таблица 2. Системные проявления язвенного колитаУ всех пациентов на фоне язвенного колита наиболее часто регистрировалась патология отделов желудочно-кишечного тракта и гепатопан-креатобилиарной системы. У каждого второго пациента регистрировалась патология костно-мышечной системы и анемия.
Современные рекомендации по диагностике и лечению хронических воспалительных заболеваний кишечника «European Crohn's and Colitis Organisation Anaemia Consensus, 2015» отмечают важность ранней диагностики, профилактики и лечения анемии у пациентов ЯК [6].
Оценена корреляционная взаимосвязь анемии с проводимой терапией. Зарегистрирована значимая взаимосвязь частоты анемии и терапии препаратами 5-аминосалициловой кислоты (5 АСК), которую получали 68 (67,3%) больных (r=0,65; p<0,01), как и при проведении сочетанной терапии препаратами 5 АСК с системными глюкокор-тикостероидами (ГКС) и/или иммуносупрессо-рами, которую получали 33 (32,7%) пациента (r=0,42; p<0,01). Подключение в 9 случаях дополнительной биологической терапии ремикейдом в стандартных дозировках (5 мг/кг массы тела) не оказывало дополнительного влияния на показатели анемии.
При анализе особенностей клинических проявлений анемии во всех случаях регистрировались общие симптомы, обусловленные развивающейся гипоксией: бледность кожных покровов и слизистых оболочек, общая слабость, головные боли, периодически ортостатическое головокружение, одышка. Были характерны жалобы, отражающие сидеропенический синдром, обусловленный тканевым дефицитом железа: сухость во рту — 12 (29,3%), ломкость и выпадение волос — 29 (70,7%), ломкость ногтей — 21 (51,2%).
Признаки возможной В12-дефицитной анемии в виде фуникулярного миелоза (онемение, чувство покалывания) отмечены только в 5 (12,2%) случаях в виде признаков симметричной нейропатии нижних конечностей с изолированными нарушениями вибрационной чувствительности, атаксией.
В полном анализе крови в 23 (56%) случаях отмечен нормальный, в 9 (22%) — средний и в 9 (22%) — низкий объём эритроцитов. Концентрация эритроцитов была достоверно ниже у больных, получавших сульфасалазин (p<0,05). Число ретикулоцитов у 26 (63,4%) пациентов было снижено, у 15 (36,6%) — нормальное.
Анализ критериев анемии у 51 пациента по классификации EORTC (Европейское общество диагностики и лечения рака), основанных на показателе уровня гемоглобина выявил лёгкую анемию (Hb 120-100 г/л) у 21 (41,2%), средней тяжести (Hb 100-80 г/л) — у 24 (47,0%), тяжёлую анемию (Hb 80-65 г/л) — у 6 (11,8%).
Все пациенты с уровнем Hb менее 80 г/л получали терапию ГКС в комбинации с иммуносупрессором. Во всех случаях процент насыщения трансферрина был менее 20%, что отражало отношение уровня железа в крови пациента к показателю общей железосвязывающей способности и являлось характерным признаком ЖДА. Насыщение трансферина железом было более низкое у больных, получавших ГКС (p<0,05) и ГКС в сочетании с иммуносупрессорами (p<0,01).
Учитывая, что у ряда пациентов при проведении ФГДС зарегистрированы маркеры субатрофи-ческого гастрита — 24 (23,8%) пациента и атрофи-ческого гастрита—21 (20,8%) пациент, а при оценке особенностей диеты выявлен крайне редкий приём морепродуктов и блюд, приготовленных из печени, была проведена оценка уровня витамина В12 иммунохемилюминесцентным методом на анализаторе IMMULITE 2000/2000 XPi. Только в 3 случаях зарегистрировано снижение уровня витамина В12, составив 106-158-180 пг/мл (референсные значения 197-771 пг/мл).
Особый интерес у пациентов ЯК представил анализ возможного формирования АХЗ. Известно, что диагностическими критериями изолированной АХЗ является уровень ферритина более 100 мкг/л. Между тем из 51 пациента с анемией у 32 (62,7%) концентрация ферритина была менее 100 мкг/л (73,0±3,9 мкг/л), что расценено как сочетание АХЗ с ЖДА.
Анализ факторов риска анемии выявил высокую частоту нарушений режима питания, её полноценности и особенностей пищевого поведения (рис. 1).
Для оценки роли полноценности рациона питания (соотношение белков-жиров-углеводов) было сформировано 2 группы у пациентов: 1-я группа — пациенты с ЯК и отсутствием на момент исследования диагностированной анемии и 2-я группа — пациенты с ЯК и анемией. У пациентов 2-й группы практически не зарегистрировано случаев полноценного пищевого рациона. Проблемы питания объяснялись частыми рецидивами заболевания и, соответственно, с частым диспепсическим и болевым синдромами, когда больные ограничивали себя в употреблении свежих овощей и фруктов (см. рис. 1).
Для пациентов с уровнем гемоглобина более 100 г/л было характерно приближение диеты к оптимальному сочетанию белков, жиров и углеводов с регулярным включением в пищевой рацион свежих овощей и фруктов.
Вторым важным фактором, способствующим формированию анемии, явилась высокая поли-морбидность этой группы пациентов, связанная, прежде всего, с патологией панкреатогепатоби-лиарной системы, формированием синдромов мальабсорбции и мальдигестии: нарушениями энтерального переваривания и всасывания.
Третьим патогенетически значимым фактором развития анемии и низкой эффективности проводимом терапии могло явиться снижение кислотности желудочного сока.
Всем пациентам с анемией, по данным амбулаторных карт и выписок из историй болезни, неоднократно проводилась её коррекция. Однако у 13 человек терапия препаратами железа была низкая и крайне непродолжительная, что потребовало анализа её причин и оптимизации терапии.
Коррекция ЖДА и восполнение недостатка железа возможно как внутривенным, так и перо-ральным путём. Фонды здравоохранения более склонны к пероральной терапии у пациентов из-за простоты дозирования, сохранения венозных сосудов для будущих сосудистых подходов и стоимости лечения. Согласно положениям ЕССО «Anaemia 2Е, EL1 (2015)», лечение препаратами железа показано пациентам ЯК при диагностированной ЖДА.
В настоящее время спектр препаратов перо-рального железа существенно расширился, что связано с необходимостью повышения их эффективности и улучшения переносимости.
Всем пациентам при регистрации анемии были назначены препараты двухвалентного железа. У 28 из 51 пациента с диагностированной анемией была достигнута её коррекция, но во всех случаях регистрировались побочные эффекты, которые сопровождались низкой приверженностью пациентов к лечению и были связаны с раздражающим влиянием неабсорбированного высокоактивного двухвалентного железа на слизистую оболочку желудочно-кишечного тракта (рис. 2).
Приём препаратов 2-валентного железы сопровождался симптомами желудочной — 13 (25,5%) и кишечной — 19 (37,3%) диспепсии, абдоминальным болевым синдромом — 9 (17,6%).
Как указывалось выше, у 23 человек терапия препаратами железа была непродолжительна в связи с низкой и/или непродолжительной эффективностью терапии. В этой группе пациентов мы оценили перспективы применения препарата гемового железа (Глибифер® форте, Бельгия), который относится к поколению новых составов для перорального приёма препаратов железа.
Существенным преимуществом препарата является повышенное всасывание гемового железа по сравнению с обычными препаратами железа благодаря специфическим механизмам всасывания в желудочно-кишечном тракте. Фиксированная комбинация гемоглобина и сульфата железа позволяла препарату не только лучше усваиваться, но и облегчала абсорбцию сульфата железа, позволяя снизить побочные эффекты со стороны желудочно-кишечного тракта.
Гемовое железо имеет природное происхождение, высокую биодоступность, удобство дозирования, независимо от приёма пищи и лекарств, снижение раздражения слизистой оболочки пищеварительного тракта, хорошую переносимость и высокую комплаентность пациента.
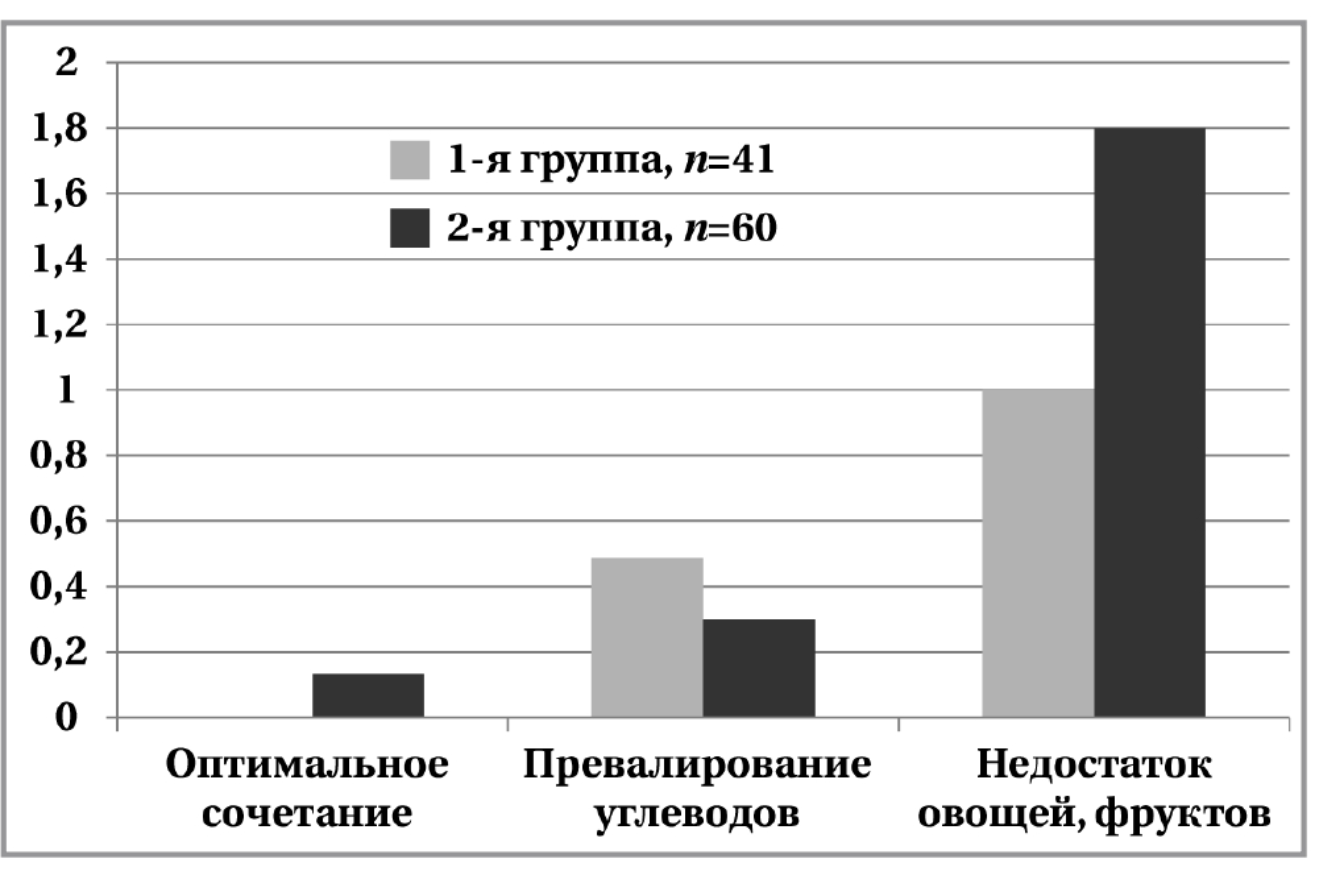 Рис. 1. Факторы риска анемии. Fig. 1. Risk factors for anemia.
Рис. 1. Факторы риска анемии. Fig. 1. Risk factors for anemia.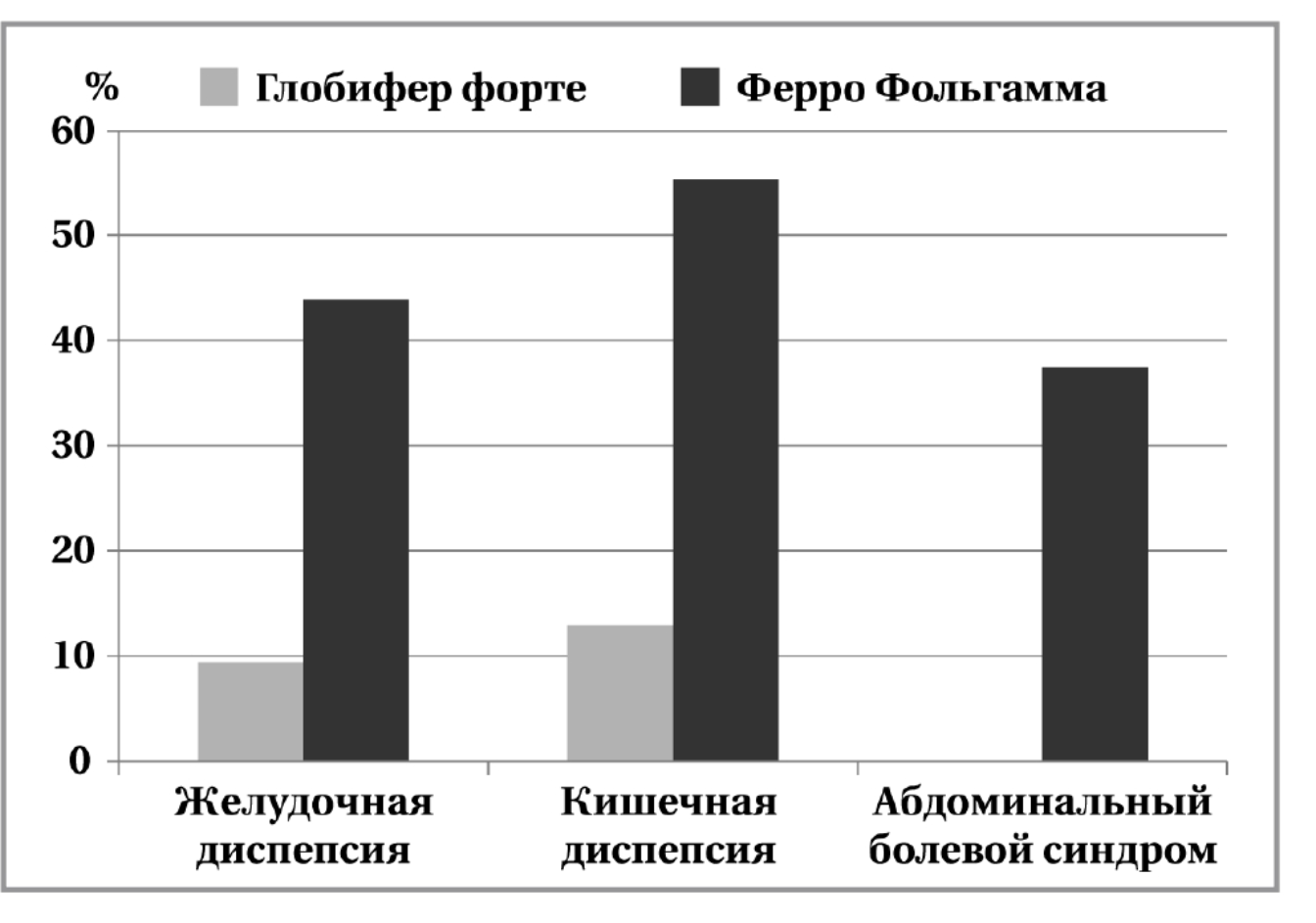 Рис. 2. Побочные эффекты продолжительной коррекции анемии пациентов ЯК
Рис. 2. Побочные эффекты продолжительной коррекции анемии пациентов ЯКВ процессе терапии отслеживалось снижение и ликвидация не только лабораторно-клиниче-ских проявлений анемии, но и улучшение качества жизни: повышение жизненных сил, бодрости и физического состояния пациентов. Важно, что препарат имеет двойной механизм абсорбции из пищеварительного тракта: эндоцитоз, опосредованный специфическими рецепторами на микроворсинках энтероцитов; прямой транспорт через гем-специфические транспортёры гемового железа способствует поглощению негемового железа и не зависит от диетических факторов.
Анализ отдалённых результатов терапии в течение шести месяцев, показали, что полипептид гемового железа имеет высокую эффективность и безопасность, что позволило избежать внутривенного введения железа, основным недостатком которого является повреждение сосудов и возникновение побочных эффектов, включая окислительный стресс, вторичный гемохроматоз.
Применение полипептида гемового железа per os является оптимальной терапевтической стратегией восстановления железа у больных ЯК. Динамика показателей представлена на рис. 3.
Важно учесть, что для пациентов с ЯК характерна высокая частота вовлечения в патологический процесс всех или большинства отделов желу-д очно-кишечного тракта, что затрудняет поступление железа, а в этом случае неиспользованное железо оказывает токсическое воздействие.
Заключение.
В большинстве случаев анемия, ассоциированная с ЯК, является сочетанием нескольких патофизиологических вариантов анемии. Наиболее значимой, несомненно, является железоде-фицитная анемия, обусловленная периодической потерей крови в связи с основной патологией, а также проблемами пищеварения и особенностями диеты пациентов.
Зарегистрирован незначительный вклад витамина В12, что можно также связать с дефектами диеты пациентов и формированием субатрофи-ческого и атрофического процесса в желудочно-кишечном тракте со снижением уровня внутреннего фактора Кастла.
Важно, что у пациентов с воспалительными заболеваниями кишечника анемия является не только лабораторным маркером хронической кровопотери, но и осложнением заболевания per se, что требует рациональных диагностических и терапевтических подходов.
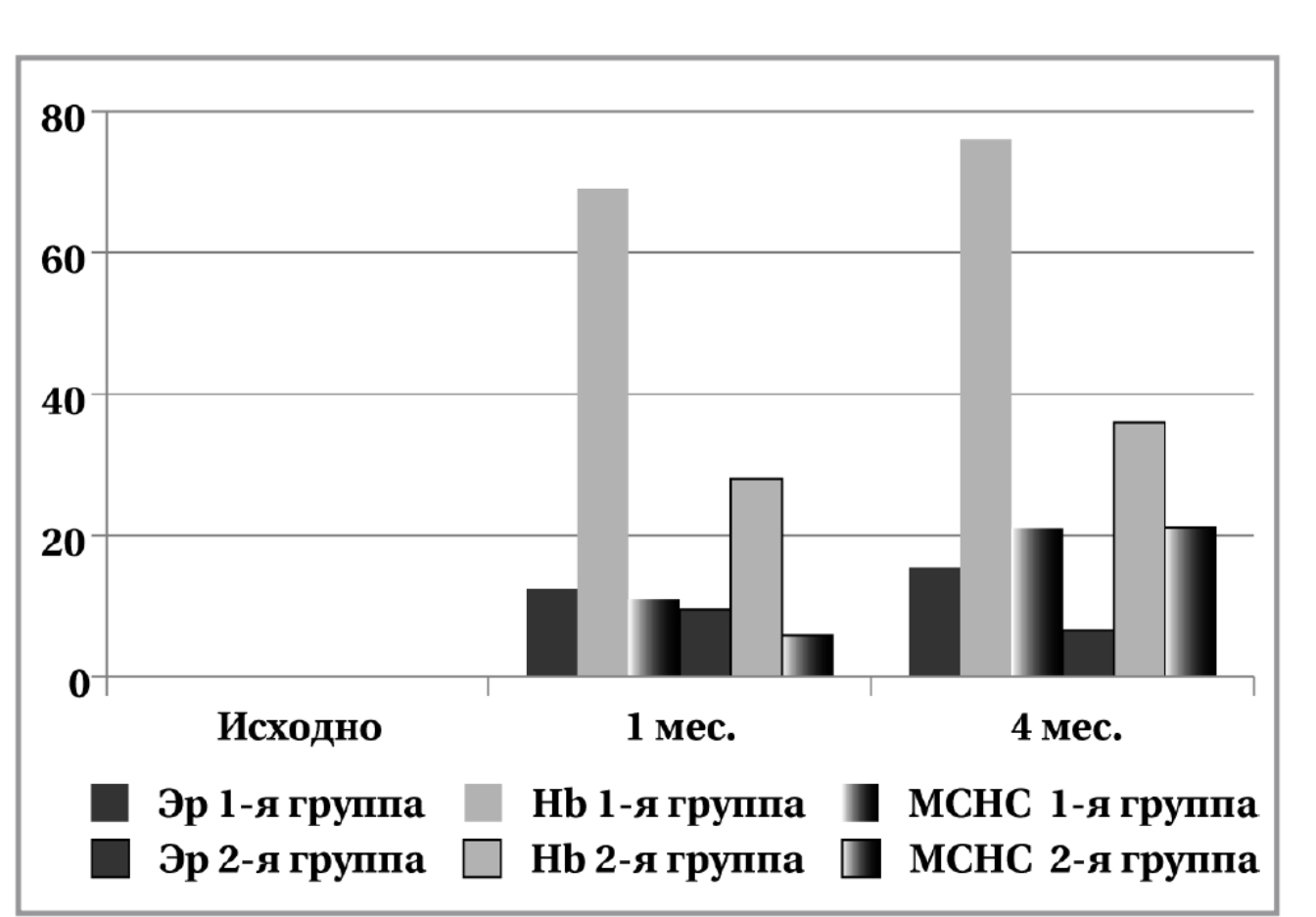 Рис. 3. Динамика прироста уровня эритроцитов, гемоглобина и средней концентрации гемоглобина в эритроците (%) на этапах реабилитации.
Рис. 3. Динамика прироста уровня эритроцитов, гемоглобина и средней концентрации гемоглобина в эритроците (%) на этапах реабилитации.Можно выделить несколько патофизиологических механизмов развития анемии у пациентов ЯК:
- хроническая кровопотеря;
- увеличение синтеза гепсидина в ответ на хронический воспалительный процесс в кишечнике с нарушением всасывания и рециркуляции железа, делая его недоступным для участия в синтезе гемоглобина;
- нарушение иммунитета с активацией про-воспалительных цитокинов(интерлейкин-1-бета, фактор некроза опухолей-альфа, интерферон-бета) и гемофагоцитоза, ухудшая доступность железа;
- проводимая терапия заболевания и, прежде всего, приём препаратов 5 АСК может также стать причиной развития ЖДА, спровоцировать развитие гемолитической анемии и мие-лодиспластического синдрома. Анемия у пациентов ЯК является частью гематологического стресс-синдрома на фоне эндогенной интоксикации, метаболических нарушений, касающихся го-меостаза железа, нарушений фагоцитоза и иммунной системы.
Применение биологически активной добавки ГлобиФер форте, представленное в электронном издании справочника Видаль 2024 г., является перспективной терапевтической стратегией патогенетической терапии анемии у больных ЯК за счёт двойного механизма абсорбции: эндоцитоз и прямой транспорт через гем-специфические транспортёры.
Дополнительная информация Конфликт интересов. Авторы заявляют об отсутствии конфликта интересов в ходе написания данной статьи.
Литература/References.
1. MolodeckyNA, Soon I.S., RabiD.M., GhaliWA., FerrisM, ChernoffG. et al. Increasing incidence and prevalence of the inflammatory bowel diseases with time, based on systematic review. Gastroenterology. 2012; 142 (1): 46-e30. doi: 10.1053/j.gastro.2011.10.001.
2. GascheC.,LomerM.C., CavillI, WeissG. Iron, anaemia, and inflammatory bowel diseases. Gut. 2004; 53 (8): 1190-1197. doi: 10.1136/gut.2003.035758.
3. Успенский Ю.П., Фоминых ЮА, Наджафова К.Н., Ведута О.И. Патогенетические механизмы формирования анемического синдрома у пациентов с воспалительными заболеваниями кишечника. Медицинский алфавит. 2021; 20: 29-34. [ UspenskijJyu.P., Fominykh JyuA, Nadzhafova K.N., Veduta O.I. Patogeneticheskie mekhanizmy formirovaniya anemicheskogo sindroma u patsientov s vospalitel'nymi zabolevaniyami kishechnika. Meditsinskij Alfavit. 2021; 20: 29-34. (in Russian)]
4. Oustamanolakis P., Koutroubakis I.E., Kouroumalis E.A. Diagnosing anemia in inflammatory bowel disease: beyond the established markers. J Crohns Colitis. 2011; 5: 381-391. doi: 10.1016/j.crohns.2011.03.010.
5. Ивашкин В. Т., Шелыгин ЮА, Абдулганиева Д.И. и др. Диагностика и лечение взрослых пациентов с болезнью Крона (Рекомендации Российской гастроэнтерологической ассоциации по лечению болезни Крона у взрослых). Российский журнал гастроэнтерологии, гепато-логии, колопроктологии. 2012; 3: 45-51. [Ivashkin V.T, Shelygin JyuA, Abdulganieva D.I. i dr. Diagnostika i lechenie vzroslykh patsientov s bolezn'jyu Krona (Rekomendatsii Rossijskoj gastroenterologicheskoj as-sotsiatsii po lechenijyu bolezni Krona u vzroslykh). Rossijskij Zhurnal Gastroenterology Gepatologii, Koloproktologii. 2012; 3: 45-51. (in Russian)]
6. Weiss G, Goodnough L. T. Anemia of chronic disease. N Engl J Med. 2005; 352: 1011-1023. doi: 10.1056/nejmra041809.
7. DignassA. U, Gasche C, Bettenworth D, Birgegard G, Danese S, Gisbert J. P., Gomollon F. et al. European consensus on the diagnosis and management of iron deficiency and anaemia in inflammatory bowel diseases. J Crohns Colitis. 2015; 9 (3): 211-222. doi: 10.1093/ecco-jcc/jju009.
8. Суржикова Г.С., Клочкова-Абельянц С.А. Белки-регуляторы метаболизма железа в дифференциальной диагностике железодефи-цитных анемий. Медицина в Кузбассе. 2022; 21 (3): 36-40. [Surzhikova G.S., Klochkova-Abel'yants S.A. Belki-regulyatory metabolizma zheleza v differentsial'noj diagnostike zhelezodefitsitnykh anemij. Meditsina v Kuzbasse. 2022; 21 (3): 36-40. (in Russian)]
9. Ershler W., Chen K, Reyes E, Dubois R. Economic burden of patients with anemia in selected diseases. Value Health. 2005; 8: 629-638. doi: 10.1111/j.1524-4733.2005.00058.
10. ГубонинаИ.В.,ЩукинаО.Б., СтукловН.И.,ГапоноваТ.В.,Абдулганиева Д.И., Князев О.В., ГубонинаН.С. Анемия при воспалительных заболеваниях кишечника: подходы к диагностике, лечению и профилактике. Альманах клинической медицины. 2019; 47 (8): 721-732. [GuboninaI.V., Shchukina O.B., StuklovN.I., Gaponova T.V.,Abdulganieva D.I., Knyazev O. V., Gubonina N.S. Anemiya pri vospalitel'nykh zaboleva-niyakh kishechnika: podkhody k diagnostike, lechenijyu i profilaktike. Al'manakh Klinicheskoj Meditsiny. 2019; 47 (8): 721-732. (in Russian)]
11. Revel-Vilk S., Tamary H, BroideE, Zoldan M., Dinari G, Zahavi I, Yaniv I., Shamir R. Serum transferrin receptor in children and adolescents with inflammatory bowel disease. Eur J Pediatr. 2000; 159: 585-589. doi: 10.1007/ s004310000491.
12. Gisbert J.P., Gomollon F. Common misconceptions in the diagnosis and management of anemia in inflammatory bowel disease. Am J Gastroenterol. 2008 May; 103 (5): 1299-307. doi: 10.1111/j.1572-0241.2008.01846.x. PMID: 18477354.
13. Галяутдинова Г.Р., Бакиров Б.А., Хисматуллина Г.Я., Гайсина Ю.И. Железодефицитная анемия как один из ведущих синдромов у пациентов с воспалительными заболеваниями кишечника. Медицинский вестник Башкортостана. 2019; 14: 1 (79): 8-11. [Galyautdinova G.R., BakirovBA, Khismatullina G. Ya, GajsinaJyu.I. Zhelezodefitsitnaya anemiya kak odin iz vedushchikh sindromov u patsientov s vospalitel'nymi zabolevaniyami kishechnika. Meditsinskij Vestnik Bashkortostana. 2019; 14: 1 (79): 8-11. (in Russian)]
14. Осипян Е.Э., Дроздов В.Н., Сереброва С.Ю., Шулятьева Н.В., Ших Е.В. Роль гепсидина в арзвитии дефицита железа при хронических заболеваниях и методы фармакологической коррекции анемии. Экспериментальная и клиническая фармакология. 2020; 83 (9): 13-19. [Osipyan E.E., Drozdov V.N., Serebrova S.Jyu, Shulyat'eva N.V., Shikh E.V. Rol' gepsidina v arzvitii defitsita zheleza pri khronicheskikh zabolevaniyakh i metody farmakologicheskoj korrektsii anemii. Ekspe-rimental'naya i klinicheskaya farmakologiya. 2020; 83 (9): 13-19. (in Russian)]
15. Болезнь Крона и язвенный колит. Под ред. Г. Адлер. М.: ГЭОТАР-Мед, 2001; 527. [Bolezn' Krona i yazvennyj kolit. G. Adler (red.). Moscow: GEOTAR-Med, 2001; 527.
16. Dignass A. U, Gasche C, Bettenworth D, Birgegard G, Danese S., Gisbert J. P., Gomollon F. et al. European consensus on the diagnosis and management of iron deficiency and anaemia in inflammatory bowel diseases. J Crohns Colitis. 2015; 9 (3): 211-222. doi:10.1093/ecco-jcc/jju009.
17. Stein J, Hartmann F., Dignas A. Diagnosis and management of iron deficiency anemia in patients with IBD. Nat Rev Gastroenterol Hepatol. 2010; 7 (11): 599-610. doi: 10.1038/nrgastro.2010.151.
О авторах:
- Чернышова Татьяна Евгеньевна — д. м. н., профессор ФГБОУ ВО ИГМА, Ижевск, Россия
- Стяжкина Светлана Николаевна — д. м. н., профессор ФГБОУ ВО ИГМА, Ижевск, Россия
- Валинуров Артур Азатович — заместитель главного врача по клинико-экспертной работе, Бюджетное учреждение здравоохранения Удмуртской Республики «Городская Клиническая Больница № 7 Министерства Здравоохранения Удмуртской Республики», Ижевск, Россия Соколова Варвара Витальевна — студент, ФГБОУ ВО ИГМА, Ижевск, Россия
ЧИТАЙТЕ ТАКЖЕ